Accumu Vol.4
放射線治療に関連して 生体に対する放射線の影響
金沢工業大学教授/京都大学名誉教授
上野 陽里
現在の癌治療には,手術を主体とする外科的治療,抗癌剤投与を主体とする内科的治療,それに放射線治療の三つの柱がある。これらはふつう併用され,学際的治療と呼ぷ。
放射線治療の最初のステップは,各種の電離粒子が衝突その他の機構で細胞内(特に細胞の生存にとって不可欠な細胞内の微小部分)にその運動エネルギーの一部または全部を与えることから始まる。そして約O.1μm以内にある分子に電離を主体とした物理的変化が起こる。ここ迄の時間は約10-15秒以内である。最後のステップは治療の成果の確認であって,少なくとも治療5年後である。放射線治療では最初に上記の微小部分で放出したエネルギーの量(同部分が吸収したエネルギーの量にほぼ等しい)と治療効果との関係だけが問題になる。この間には無数の化学的,生物学的,社会的修飾因子が介在する。
吸収線量
これらの修飾因子は,入力側である放射線に関連するものと出力側である癌に関連するものに大別される。ここでは前者の一部を説明する。放射線治療では癌に吸収されるエネルギー量が最も大切な基本因子である。これを吸収線量(J/kg,単位名グレイ,Gy)という単位で表現するが,これは物質中の平均的な線量で,ある一点の線量ではない。
さて放射線治療には問題点がある。それは,正常組織に放射線を与えず癌だけに放射線を与えることはできないということである。放射線治療の歴史をこの問題の改良の歴史と言っても差し支えない。治療効果を上げるためにできる限り多量の吸収線量を癌に与え,その他の正常組織にはできる限り少ない吸収線量を与えるにはどうすればよいか。この命題のために実に多くの努力が払われている。
まず正常組織の線量を少なくする医学的方法として,癌を手術的に露出させて照射する術中照射法がある。これはよい治療効果を上げており,京都大放射線科の得意とする手法の一つである。しかしそれでも癌の向こう側の組織は,光子を利用する限り必ず照射されるのでふつう電子を使用する。
物理的方法による改善は,古くから行われてきた。最も簡単なものは,皮膚から盛り上がった癌に接線方向から照射する方法であり,癌より深部の組織の照射を避けることができる。また癌には放射線が集中するが,その前後の組織には集中しないように,照射を分けて且つ多方向から照射する多門照射法がある。これを更に発展させたものが,放射線を円の中心に向けて放出するようにした装置を癌を中心に設置して円形に回転させる回転照射法である。この方法では癌は回転中照射を受け続けるが照射を受ける他の組織は時々刻々移動する。常に照射を受け続ける回転中心部分は球形になるが,癌は球ではない。不整形である癌の形に沿って照射を継続したい。その希望に応えたものが原体照射法である。このためには,回転しながら時々刻々放射線束を変化させる装置が必要であり,その前提は癌の形と位置を二次元,三次元にシミュレートできなければならない。次の方法は,癌の吸収線量を癌の前方にある皮膚の吸収線量に対して相対的に-相対的にである-多くするためにエネルギーの高い光子を使用するものである。これは光子のエネルギーを高めることによって癌より前の組織での吸収による減少を抑えるためである。但し癌の前後の組織の吸収線量は増加するし,ビルド・アップ効果という治療に邪魔な現象も出現する。しかし多門照射や回転照射と組み合わせたリニアックと呼ばれる装置からの高エネルギーX線は治療効果がよいので広く使用されている。
近年粒子科学の進歩によって多種多様な大型の粒子を治療に利用できるようになった。これらの粒子を使用する場合に一つの問題が生じる。それはこれらの粒子では平均値である吸収線量(測定値)が物質中のある一点の吸収線量を代表しなくなることである。この両者のズレを治療ではRBEという言葉で表現している。但し放射線生物学でいう厳密な意味でのRBEでない。前者が後者より小さいので,一見少ない線量で効果が上がるようになる。これは治療時間の短縮になるので有利な特徴である。まず比較的簡単な,また安価な装置で発生する電子(RBEは1)があり,浅在性の癌の治療に各病院で広く利用されている。治療用速中性子はRBEはほぼ3である。癌の前後の組織への照射による吸収線量は大きいため,組織の障害を避けて癌に十分な吸収線量を与えることができるなどの難点のため期待した程の効果がない。π-中間子は京都に深い関わりのある粒子である。湯川教授もこの医学利用に強い関心を示しておられた。π-粒子はその走行の終点で物質原子の核破砕を起こしてスターといわれる高密度のエネルギーの放出を局在性に起こすので,この部分を癌に一致させて治療を行うものである。従ってその前後の組織の吸収線量は相対的にも絶対的にも極めて少ない筈である。しかしこれとても良い事ずくめではない。一つの問題はπ-粒子が放出されると同時に電子,μ-粒子,π+粒子等が放出され,それらによる正常組織の吸収線量は少なくない。現在π粒子治療を実際に行っているのはスイスだけであるが,それなりの治療効果を上げている。
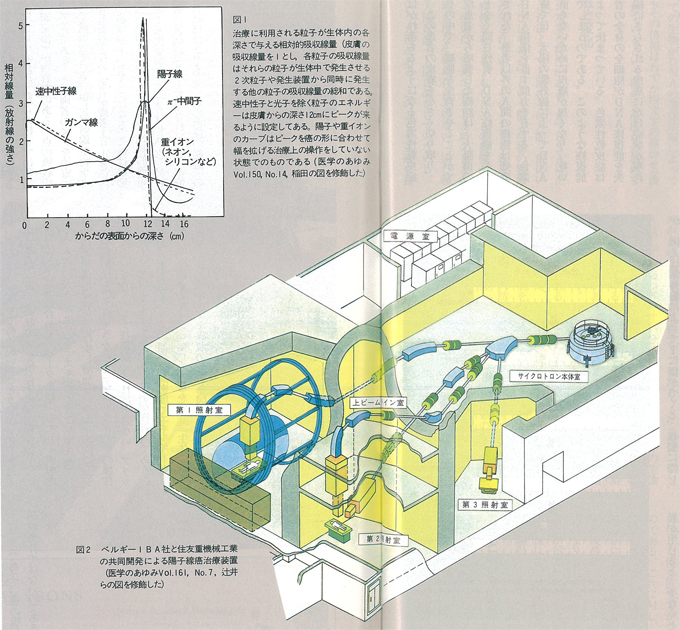
治療に使用される粒子としてもう一つ重要なものは陽子である。陽子の特徴は,治療の立場から述べるならば,ブラッグ・ピークが極めて高く鋭いこととカーブがピークの後で尾を引かず従って吸収線量を殆ど与えないことである。実際には癌の大きさに合わせてピークを拡大したり,照射中ピークを癌の大きさに合わせてスキャンさせたりするので,癌前後の組織の吸収線量は少し増加する。また純粋に陽子だけを放射することはできない。このようなピークの操作は高度なシミュレーション技術がなければできない。ブラッグ・ピークとはエネルギーが均等な粒子が物質内である距離を走ってから停止し,その部分に高密度でエネルギーを放出して吸収線量のピークを生じることをいう。生体内に入った粒子からのエネルギー吸収の分布を図1に示す。
もう一つの利点は陽子が電荷を持っているために,外側の電場を変化させることで陽子の走る方向を自由に変えられることである。これによって陽子の線束を針のように鋭く絞り込める。これらの特性のために陽子のRBEが光子と殆ど変わらないにも拘らず陽子治療への期待が大きい。実際今日の放射線治療では陽子治療は最良の効果を上げている。また陽子治療装置はπ中間子のそれに比べて非常に安価である。陽子治療装置はまだ関西地区にはなく,その設置が強く期待される。最近我が国で小型の陽子治療装置が開発されたので,そのレイアウトを図2に示した。
本稿では吸収線量だけ簡単に述べたが,治療では,物理的諸条件の設定以外に患者の生活条件,健康状態,癌の状態,癌の種類,癌細胞と正常細胞の放射線生物学的性質,癌の位置等を考慮しながら,癌により多量の吸収線量を与えなければならない。放射線治療の最終目的は治療後の患者の「生活の質」-Quality of Life-をより高く維持することであって,癌の吸収線量が大きいことは最優先する治療条件ではないのである。